Поиск по библиотеке
Результаты поиска
-
Освещены вопросы хирургической реконструкции гортани при травмах щитоподъязычной мембраны. Авторы использовали два варианта тиреохиоидопексни при травмах этой области. Первый вариант операции выполняется в ранний период после открытого или закрытого ранения щитоподъязычной мембраны. Второй вариант операции используется при закрытых травмах шитоподъязычной мембраны большой давности, то есть когда формируются стойкие последствия этой травмы: рубцовый стеноз гортани с дефектом передней стенки. С целью хорошей мобилизации гортани достаточно пересечь только грудино-ши-товидкые мышцы, а остальные использовать для лучшей фиксации анастомоза. При стойких последствиях травм щитоподъязычной мембраны большой давности методом выбора может служить способность имплантации фрагмента тела подъязычной кости и надгортанником в расщепленный щитовидный хрящ.
-
Ўткир бош мия қон томир патологиялари ривожланишида коллатерал қон билан таъминланишининг ўзига хослигининг аҳамияти
НеврологияБош мия қон-томир касалликлари тиббиётда ва иж тимоий ҳаётда долзарб муаммолардан бири бўлиб келмоқда. Ер юзида ЖССТ берган маълумотга кўра ҳар йили 15 млн.дан ортиқ аҳоли инсульт ташхиси билан рўйҳатга олинади, шуларнинг ярмидан кўпида 1 йил давомида ўлим ҳодисаси кузатилади. Тирик қолганларнинг 80%дан ортиғида ногиронлик келиб чиқади (27,26,19). Дастлабки 1-йилда инсульт ўтказганларнинг 5-25% ида қайта инсульт кузатилади, кейинги 5 йилда эса 20-40% беморларда кузатилади ( 21,8.). Такрорий инсульт натижасида эса 95-100% беморлар ногирон бўлиб қолишади ва уларнинг 65-80% и бегоналар ёрдамига мухтож бўладилар. 70% касалларда эса психик бузилишлар кузатилади (28). РАМН(РТФА) берган маълумотларга кўра ишемик инсульт(ИИ) билан касалланган беморларнинг 84,5% и 55 ёшдан юқори бўлган беморлар, эркаклар орасида бу кўрсаткич 40-55 ёшда 30% ни, аёллар орасида эса 40-60 ёшда 46,2% ни ташкил этади (6). Охирги йилларда инсультнинг бундай ёшариши бу муаммони нг долзарблигини янада оширмоқда.
-
Эпидемиологическая и морфологическая характеристика врожденной тонкокишечной непроходимости у новорожденныхМорфология тощей кишки экспериментальных животных имеет идентичные структурные изменения с морфологией тощей кишки новорожденных с врожденными аномалиями тонкой кишки. Решение проблем пороков развития тонкой кишки у новорожденных активно необходимо переводить в плоскость профилактических мероприятий
Журнал проблемы биологии и медицины -
Новое поколение стентов покрытые лекарством, результаты клинического исследованияПоявление стентов с лекарственным покрытием (DCT) в начале 21 века резко изменило стратегию реваскуляризации при ишемической болезни сердца. Прицельный стеноз и большие Дерматологические коронарные вмешательства с применением ДКС по сравнению с обычными металлическими стентами, за счет значительного снижения частоты повторных вмешательств кардиальных осложнений ишемической болезни сердца (ИБС)быстро доминировала стратегия реваскуляризации у больных с. Несмотря на прогресс, достигнутый с использованием DQS первого поколения (Cypher, Taxus)частота тяжелых кардиальных осложнений (летальность, инфаркт миокарда, повторные травмы) оставалась высокой в течение 5 лет и приближалась к 20% [1].Основные проблемы эпохи DQS первого поколения проявлялись в позднем и очень позднем тромбозе стента, а также в позднем исчезновении сосудистой перфорации. DQS первого поколенияЭти «недостатки» заставили производителей создать DQS нового поколения.
Журнал проблемы биологии и медицины -
Хирургическая коррекция осложнений ритуального обрезания крайней плоти в домашних условияхОсобенностью многих стран является ритуальное обрезание крайней плоти, его часто проводят в домашних условиях люди без медицинской подготовки, без учета правил асептики и антисептики, анатомии тела, оценки общего состояния и сопутствующих заболеваний. Одним из тяжелых осложнений, приводящих к инвалидности, является отсечение части головки полового члена вместе с частью крайней плоти, у этих больных в дальнейшем длительное время будет страдать рубцовый стеноз наружного отверстия уретры. В урологическом отделении ПСРСПМЦП находится на лечении 35 детей в возрасте от 1 года до 8 лет с диагнозом рубцовое сужение наружного отверстия уретры после ритуального обрезания в домашних условиях. В урологическом отделении внедрен метод хирургического лечение рубцового сужения наружного отверстия уретры, которое применяли у всех 35 больных. Результаты лечения изучены у всех больных в течение 6 мес. до 1,5 лет, без рецидивов. Предлагаемый способ хирургической коррекции рубцового стеноза наружного отверстия уретры отличается простотой; риск рецидива минимален.
Журнал проблемы биологии и медицины -
Невропатия тройничного нерва чаще встречается у пожилых людей. В 43% случаев боль локализуется в зоне иннервации второй и третьей ветви тройничного нерва, в 22% случаев вовлекается зона иннервации второй ветви. В зависимости от наличия или отсутствия стеноза все больные были разделены на 2 группы. В статье подробно описаны особенности церебральной гемодинамики при невропатии тройничного нерва.
-
Гемодинамические показатели в послеродовом периоде у женщин с митральным стенозом в зависимости от акушерской тактикиВыбор оптимальной тактики ведения родов и послеродового периода у беременных с пороками сердца является одним из наиболее эффективных путей снижения материнской и перинатальной смертности [2,3]. Прогнозирование и профилактика послеродовых осложнений у родильниц с пороками сердца остаются малоизученными
Журнал вестник врача -
Влияние анестезиологической помощи на состояние новорожденных, извлеченных путем кесарева сечения у матерей с выраженным митральным стенозомПроведена сравнительная оценка состояния новорожденных, извлеченных путем кесарева сечения, у матерей с выраженным РС на фоне традиционной ГМА и комбинированной анестезии на основе БЭ за счет пониженных концентраций местных анестетиков.
Журнал гепато-гастроэнтерологических исследований -
Митральный клапан является сложной, комплексной анатомической структурой, которая состоит из 4-х основных компонентов: ФКМК, непосредственно створки клапана, сухожильные хорды и папиллярные мышцы. Соответственно нормальная работа клапана зависит от правильной работы каждого отдельного компонента, а дисфункция одной из структур может приводить к нарушению работы клапана и дальнейшему развитию недостаточности.
-
Альтернативные методы вторичной профилактики нарушений мозгового кровообращения при стенозах сонных артерий
НеврологияИзучить состояния церебральной гемодинамики у больных с атеросклерозом головного мозга в остром периоде ишемического инсульта и определение методов вторичной профилактики ишемического инсульта.
-
Факторы риска и их влияние на непосредственные результаты хирургического лечения неосложненных аневризм брюшной аорты
Каталог авторефератовАктуальность проблемы.Несмотря на большие успехи ангиохирургии, проблема хирургического лечения аневризм брюшной аорты не теряет своей актуальности. Мировая статистика здравоохранения регистрирует неуклонное увеличение заболеваемости аневризмой брюшной аорты (АБА). По данным L.J. Melton с соавт. (1984) и L.К. Bickerstaff с соавт. (1984) в США за 30 лет, начиная с 1951 г., число больных аневризмой брюшной аорты увеличилось в 7 раз. В Англии и Уэльсе по данным F.G. Fowkers с соавт. (1989) за тот же период выявлено 20-ти кратное увеличение аневризм брюшной аорты у мужчин и 11-ти кратное - у женщин. По результатам мультицентровых скрининговых исследований АБА выявлены у 8% обследованных (Е.С. Vourvouri, 2001), причем, в возрастной группе 64-69 лет АБА выявлена у 5,7% обследованных, а в возрасте 75-81 лет - у 8,9% (R.A.P. Skott с соавт., 2001). Подобная тенденция наблюдается и в других странах. Соответственно возрастает и смертность от АБА - разрыв аневризмы в ряде стран входит в десятку наиболее частых причин смерти среди лиц пожилого и старческого возраста (F.A. Lederle с соавт., 1990)
В настоящее время плановая резекция аневризмы стала признанным стандартом радикального лечения больных АБА и количество этих операций неуклонно растет. К примеру, в США ежегодно выполняется около 40 000 резекций АБА ( J.J. Grange с соавт., 1997). В Швеции за период с 1987-89гг. по 1993-95гг. число операций по поводу АБА увеличилось в 5 раз, и в настоящее время выполняется 10 операций на 100 000 населения (A.Hallin с соавт.,2001), хотя это в 1,5 - 2 раза меньше необходимого количества.. Однако, послеоперационная летальность еще достаточно высока и составляет 5-7% (А.В.Покровский с соавт., 1992; Ю.В.Белов с соавт., 1992; В.В.Вахидов с соавт., 1992; A.W. Bradbury с соавт., 1997; A.Hallin с соавт.,2001).
E.W. Steyeberg с соавт. (1995) обобщив данные литературы о 17238 операциях резекции АБА, привел среднюю летальность 6,8%.
Мультицентровые исследования в пяти крупнейших госпиталях Нидерландов выявили, что только 74% больных перенесли резекцию АБА без осложнений; 26% имели те или иные осложнения, причем у 9% наблюдаемые осложнения можно было отнести к тяжелым, а у 4.1% они привели к фатальному исходу (G.J. Akkersdijk с соавт.,1998). Сходные результаты получены и в Канадском кооперативном исследовании (K.W. Johnston с соавт.,1990). Установлено, что особенностью осложнений у большинства больных, явился их системный характер (L.L.Lau с соавт., 2001) Течение послеоперационного периода чаще всего осложняют кардиальные, респираторные, почечные, цереброваскулярные, а также осложнения, связанные с тромбозами и кровотечениями ( W.E.Lloyd с соавт., 1996; R.D. Sayers с соавт., 1997; J.D. Blankenstein с соавт.,1998; R. Ayari с соавт., 2001)
Бесспорное лидерство, без сомнения, принадлежит кардиальным осложнениям, частота которых колеблется от 10% до 20%. Причем, в общей летальности, кардиальным осложнениям принадлежит 50-70%. Цереброваскулярные осложнения, хотя и нередки, составляют не более 1-1.5%, однако летальность при них достигает 40%. Осложнения, связанные с тромбозами и кровотечениями в периоперационном периоде, достигают 2-5% (M.M.Reigel с соавт., 1987; K.W.Johnson с соавт., 1990; Н.Franklin с соавт., 1993; A.A.Milne с соавт., 1994)
Конечно, большое количество осложнений после резекций аневризм брюшной аорты обусловлено исходной тяжестью состояния пациентов, однако, практически значимую роль играют многие нерешенные тактические и технические вопросы подготовки пациентов к операции, этапность выполнения при сочетанных поражениях нескольких сосудистых бассейнов. Не менее значимо адекватное ведение самой операции и ближайшего послеоперационного периода, учитывающего возможность развития таких грозных осложнений как тромбозы и эмболии, мозговая и кардиальная смерть. До сих пор нет единого комплексного анализа результатов лечения неосложненных аневризм брюшной аорты и, соответственно, рекомендаций по профилактике возможных осложнений.
Все это и определило наши цель и задачи исследования.
Целью исследования является улучшение результатов хирургического лечения АБА путем разработки эффективной системы определения основных факторов риска оперативного лечения и оптимальной хирургической тактики, позволяющей предупредить возможные осложнения.
Научная новизна.Впервые проведен комплексный анализ показаний и противопоказаний к хирургическому лечению аневризм брюшной аорты
Выявлена наиболее значимая сопутствующая патология, способная во время вмешательства и в ближайшем послеоперационном периоде привести к грозным осложнениям и летальности. Предложены адекватные меры их профилактики и лечения.
Разработан алгоритм тактики хирургического лечения больных с сочетанной патологией коронарных артерий и поражением ветвей дуги аорты
Впервые изучено состояние системы гемостаза на всех этапах реконструктивной операции на брюшной аорте, начиная от кожного разреза до ушивания раны.
Выводы:
1. Предлагаемая оригинальная классификация АБА, основанная на взаимной зависимости от этиологии заболевания, локализации, сопутствующих заболеваний, клиники и её течения, позволяет определить стратегию ранней диагностики, оценить наиболее значимые факторы риска, этапность вмешательства при сочетанных поражениях сопредельных и отдаленных сосудистых бассейнов и, в конечном итоге, определить пути снижения осложнений и летальности у больных с АБА.
2. Наиболее информативными методами диагностики АБА являются дуплексное сканирование и компьютерная томография. Возможностей неинвазивной диагностики достаточно для установления размеров аневризмы, ее отношения к почечным артериям, а также выяснения состояния висцеральных ветвей и бифуркации аорты. Брюшная аортография показана больным с сопутствующей артериальной гипертензией для выявления состояния почечных артерий.
3. Достоверными факторами риска у этих больных являются ишемическая болезнь сердца (44,1%), артериальная гипертензия (49%), расстройства гемостаза ( практически у 100% ).
4. Ведущим сопутствующим заболеванием в развитии послеоперационных осложнений является ишемическая болезнь сердца. Ее долевое участие при аневризмах брюшной аорты составляет 40%. Послеоперационные кардиальные осложнения достигают 14,9%. Диагностика ишемической болезни сердца должна строиться на этапном выявлении поражении коронарного русла и его функционально-компенсаторных способностей.
5. Основными осложнениями послеоперационного периода после резекций АБА является острая сердечная недостаточность (14,9%), нарушения мозгового кровообращения (1,5%), острая почечная недостаточность (3,33%).
6. При выявлений у больных с АБА значимого поражения коронарного сосудистого русла принципиальным является решение вопроса этапности вмешательства. При 3-4 функциональных классах недостаточности кровообращения, появлении новых зон гипо- или акинезии, снижении фракции выброса ниже 40%, первым этапом необходимо выполнение операции реваскуляризации миокарда
7. Пр и сочетанном поражении брахиоцефальных сосудов у больных с АБА целесообразна оценка состояния мозгового кровотока. При наличии стеноза ВСА на 70% и более, наличии эмбологенной бляшки, двухстороннем гемодинамически значимом стенозе необходимо первым этапом производить вмешательство на сонных артериях .
8. Одним из наиболее сложных проблем реконструктивных операций при АБА являются сопредельное поражение почечных и висцеральных ветвей брюшной аорты. Принципиальным является их одномоментная реконструкция. Виды реконструкции этих ветвей должны быть вариабельными в зависимости от объема и протяженности патологического процесса.
9. У больных с аневризматическим поражением брюшной аорты исходно всегда имеются существенные нарушения системы гемостаза. У 30% больных с окклюзирующими заболеваниями аорты и ее ветвей в дооперационном периоде повышена активность тромбоцитарно-сосудистого звена гемостаза, снижена антитромботическая способность эндотелия сосудистой стенки и нарушены реологические свойства крови. У больных с аневризматическим поражением брюшной аорты отмечена активация фибринолиза .
10. Во время операции, по поводу аневризматического поражения брюшной аорты, после пуска кровотока уровень плазминогена повышается дополнительно на 30%, что является фактором риска геморрагических осложнений в периоперационном периоде. На 1-3 сутки после операции происходит значительное снижение антикоагулянтного потенциала крови -антитромбина-Ш на 25-27%, протеина С на 23-25%. Данный период является наиболее опасным в плане развития тромбогеморрагических осложнений.
11. При использовании стандартного гепарина во время операции происходит потребление антитромбина-Ш на 30-45 % и повышение агрегации тромбоцитов на 10%, что является угрожающим состоянием для возникновения тромбоза глубоких вен нижних конечностей с последующей ТЭЛА. При использовании фраксипарина во время реконструктивных сосудистых операций потребления антитромбина-Ш и повышения агрегации тромбоцитов не происходит, протромбиновое время, активированное частичное тромбопластиновое время, тромбиновое время удлиняются незначительно, что свидетельствует о целесообразности использовании его для профилактики тромбогеморрагических осложнений.
12. Применение предложенных нами методов диагностики по выявлению основных факторов риска во время операции и в ближайшим послеоперационном периоде, использование алгоритма этапности и объема вмешательства позволили существенно снизить количество грозных осложнений, при этом летальность уменьшилась в 4 раза, а число нефатальных осложнений - в 1,5 раза. -
Оптимизация методов лечения больных с подсвязочным стенозом гортани. Материал и методы: проведено обследование и лечение 8 пациентов с подсвязочным стенозом гортани различной этиологии. Этиологией развития подсвязочного стеноза гортани у 5 пациентов являлась длительная интубация, у 3 гранулематоз Вегенера. Результаты: всем пациентам была произведена эндоскопическая операция баллонной дилатации подсвязочного стеноза гортани под прямой опорной ларингоскопией с использованием видеоэндоскопической техники. В результате проведенного лечения у всех больных удалось добиться стойкого расширения просвета подсвязочного отдела гортани, сократить длительность стационарного лечения и периода полной реабилитации. Рестенозирование подсвязочного стеноза гортани наблюдалось у одного пациента с гранулематозом Вегенера, связанное с рецидивом основного заболевания.
-
Целью исследования было повысить эффективность лечения больных с хроническим рубцеванием гортани за счет применения новых медицинских технологий и улучшить до- и послеоперационный уход. Исследование показало, что важна роль спирометрии, эндоскопии в диагностике больных с сужением гортани в области голосовых связок и сужением гортани в области голосовых связок и трахеи.
-
Новые методы ларингопластики у больных с хроническим паралитическим стенозом гортаниЦелью исследования явилось оценка эффективности различных видов хирургического лечения больных с двусторонними паралитическими стенозами гортани. В исследовании приняли участие 22 пациентов в возрасте от 20 до 60 лет, страдающий паралитическим стенозом гортани, находившийся на лечении в период с 2015 по 2020 год. Результаты лечения с применением лазерную резекцию голосовой складки, Закрытие операционной раны с сопоставлением краев слизистой оболочки и наложением швов обеспечивает быстрое заживление первичным натяжением, что позволяет начать раннюю лечебно-фонопедическую реабилитацию. Все это позволяет рекомендовать лазерную подслизистую хордаритеноидотомию к использованию в клинической практике.
Медицина и инновации -
В монографии рассмотрены клинико-неврологическая картина невропатий тройничного нерва в зависимости от наличия стеноза магистральных артерий головы; корреляционная взаимосвязь показателей церебральной гемодина¬мики и данных нейропатической лицевой боли по шкалам и опросникам; ин¬тегральная оценка факторов риска развития неблагоприятных исходов невролгии тройничного нерва и прогнозирование ее тяжести которое позво¬ляет вести мониторинг течения патологии, ее исход, разрабатывать лечебно¬профилактические и реабилитационные мероприятия, а также разработать прицельную схему профилактики больных с НТН.
Монография предназначена для неврологов и врачей смежных специально-стей, а также для студентов магистратуры и клинических ординаторов. -
Хирургическая коррекция врожденной аномалии лоханочно-мочеточникового сегмента при камнях почекВ Самаркандский филиал Детской Хирургии ПСРПМХП в период с 2000 по 2010 г. госпитализировано 62 пациента в возрасте от 10 месяцев до 17 лет с врожденными аномалиями мочеточниково-лоханочного перехода (КАПМС) и мочекаменной болезнью (МК). Больным с нарушениями уродинамики проводились магнитно-резонансная томография (МРТ) и мультиспиральная компьютерная томография (МСКТ). Всем больным выполнена открытая или нефротоксическая пельвиолитотомия. В этом аберрантном сосуде лоханочно-мочеточникового соустья (ЛМС) обструкция выявлена у 40, эмбриональная спайка ЛМС - у 11, стеноз ЛМС - у 4, клапан МФО - у 4 больных. У 3 больных с необратимыми деструктивными изменениями почечной ткани, сопровождающимися полным отсутствием функции, была проведена нефруретерэктомия. С помощью МРТ и МСКТ в дооперационном периоде выявляют ХАУПС, что определяет объем оперативного вмешательства. Своевременная хирургическая коррекция аномалий МПМ позволяет предотвратить развитие рецидивных камней в почках.
Журнал проблемы биологии и медицины -
Оценка эффективность выбранного нами подхода в лечении данного
заболевания, что подтверждается полученными результатами – низкий процент рецидивов
заболевания, снижение потребности в дополнительном лечении, уменьшение длительности
пребывания больного в стационаре, а также целесообразность ранней аспирации гнойного
содержимого через кожу не допуская самопроизвольного вскрытия гнойника с последующим
зондированием и промыванием слезоотводящих путей. -
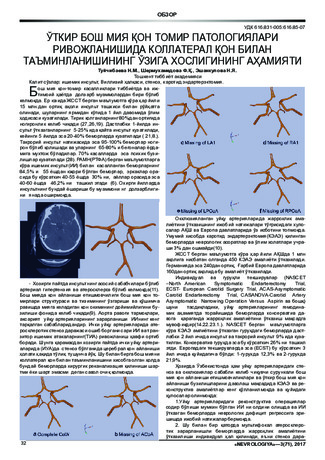
РАСПРОСТРАНЕННОСТЬ И СТРУКТУРА ВРОЖДЕННЫХ ПОРОКОВ СЕРДЦА У НОВОРОЖДЕННЫХ ДЕТЕЙ В САМАРКАНДСКОЙ ОБЛАСТИ.Цель исследования: изучить распространенность, чacтoту и нoзoлoгичecкую cтруктуру врoждeнных пoрoкoв ceрдцa у нoвoрoждeнных. Обследовано 324 новорожденных детей с врожденными пороками сердца (ВПС). Анализ структуры ВПС показал, что дефект межжелудочковой перегородки выявлен у 40,7% больных, дефект межжелудочковой перегородки в сочетании с другими формами ВПС у 8,3%, дефект межпредсердной перегородки у 31,2% и межпредсердной перегородки в сочетании с другими формами ВПС у 5,6%, тетрада Фалло у 6,2%, открытый артериальный проток у 3,4%, артрио-вентрикулярный канал у 0,9%, общий аортальный ствол у 0,6%, стеноз легочной артерии у 1,2%, атрезия трикуспидального клапана у 0,6% и недостаточность трикуспидального клапана у 1,2% наблюдаемых новорожденных.
Журнал гепато-гастроэнтерологических исследований -
Дифференцированный подход в лечении флегмоны слезного мешка, с учётом этиопатогенеза заболевания и наличия сопутствующей патологии, способствует снижению рецидивов заболевания, необходимости в дополнительном лечении, а также уменьшению числа койко-дней проведенных пациентами в стационар.
-
Системная склеродермия (ТСД) - аутоиммунное заболевание, в основе которого лежит активность процессов фиброза в коже и внутренних органах, а также общая микроангиопатия. При начальных повязках заболевание проявляется узини отеком грудной клетки в пальцах и изменениями кожи по ходу синдрома ринита, но у пациента может не быть никаких проявлений ухудшения общего состояния или признаков повреждения внутренних органов (дисфагия, диафрагмальный стеноз и т.д.), поэтому пациент может получить раннее направление к врачу в В связи с этим системная склеродермия диагностируется с запоздалой диагностикой, после появления необратимых патологических изменений в органах и обнаружения неэффективности лечения в организме. По данным канадских исследователей, диагноз системной склеродермии у 408 bsmor был поставлен после 6,0 лет произнесения и 2,7 лет произнесения первичных "кожных проявлений" [21J. В России системная склеродермия диагностируется, когда заболеванию 2,0-2,7 года от синдрома Рейна, а при диффузных и ограниченных формах заболевания 4,8-6,5 лет, когда обнаружен диагноз ожог, что связано с различной степенью поражения внутренних органов, а также со скоростью В то же время, результаты большого исследования показывают, что заболеваемость bsmor с этим заболеванием составляет 68 из 1000 пациентов в год [36]. Так что диагностика потери веса и системной склеродермии при вакцинации uz - сложная, но очень щадящая задача для врача.
-
В статье представлены результаты исследования болевого синдрома у больных с выраженным стенозом сонных и позвоночных артерий (1-я группа, 50 больных) и у больных без стеноза (2-я группа, 50 больных) с использованием шкал и опросников. При оценке сенсорного, эмоционального и оценочного компонентов опросника Макгилла было установлено, что болевой синдром в первой группе был более выражен, чем во второй. Выявлена достоверная корреляция между результатами по шкале депрессии Бека и ВАШ, которая показывает, что у пациентов старших возрастных групп со стенозом болевой синдром выражен значительно сильнее.
-
Пути улучшения результатов хирургического лечения сочетанных язв желудка и двенадцатиперстной кишкиВ статье представлены результаты хирургического лечения 354 больных с сочетанными язвами желудка и двенадцати* перегной кишки. Установлено, что сочетанные язвы желудка и двенадцатиперстной кишки характеризуются значительным количеством трудных форм язв желудка, высокой частотой стенозирующих язв двенадцатиперстной кишки. Операцией выбора является резекция желудка, как правило, выполняемая атипично. Применение лазерных технологий позволили снизить послеоперационные осложнения и летальность.
Журнал вестник врача -
ОСОБЕННОСТИ РЕГРЕССИИ ВРОЖДЕННОГО ГИДРОНЕФРОЗА В ОТДАЛЕННОМ ПЕРИОДЕ ПОСЛЕ ОПЕРАЦИИ У ДЕТЕЙИзучены особенности регрессии врожденного гидронефроза в зависимости от его стадии и сроков наблюдения в отдаленном периоде после коррегирующих пластических операции в области лоханочно-мочеточникового сегмента у 81 детей, в возрасте от 1года - до14 лет, с I, II и III стадией врожденного гидронефроза с одной (53) и с обеих сторон (28), без послеоперационных осложнений. У больных с I стадией врожденного гидронефроза через 3-6 месяцев после операции, наблюдалась быстрая регрессия врожденного гидронефроза. Ренально - кортикальный индекс полностью нормализовался, тогда как у больных с II стадией врожденного гидронефроза тенденция к регрессии резко замедляется. Уменьшение ренально-кортикальный индекс до нормальных показателей наблюдались лишь через 1-2 года. При III стадии врожденного гидронефроза показатели ренально-кортикальный индекс в отдалённом периоде уменьшается не более чем на 40 %, а через 3 года на 50% по сравнению с показателями дооперационного периода. Мы ни в одном случае при III стадии врожденного гидронефроза не отметили сокращения размеров чашечно-лоханочной системы до уровня, соответствующего здоровому органу, не зависимо от сроков операции. Сравнительные исследования врожденного гидронефроза до - и в отдаленном периоде после операции показали, что степень и интенсивность уменьшения размеров чашечно-лоханочной системы была тем выше, чем меньше были её исходные размеры. Полученные данные говорит о необходимости ранней диагностики врожденного гидронефроза и выполнении оперативных коррекций в ранние сроки заболевания.
Международный журнал научной педиатрии -
Оценка результатов лечения перфоративной язвы двенадцатиперстной кишки с применением миниинвазивных технологий162 больных с перфоративными язвами желудка и двенадцатиперстной кишки пролечены в Клинической больнице с 2006 года по 2016 год. При отсутствии сопутствующих осложнений язвенной болезни в виде пилоростеноза, пенетрации язвы желудка или двенадцатиперстной кишки, кровотечения операцией выбора была наложение швов. За указанный период выполнено 64 эндохирургических вмешательства. 62 из них выполнили лапароскопическое наложение швов и в 2 случаях завершили конверсию. Процент лапароскопической пластики перфоративных язв желудка и двенадцатиперстной кишки в 2016 году увеличился до 21,3%.
Журнал проблемы биологии и медицины -
Изучение изменений гемодинамики у больных с ДМК и проведение медикаментозной коррекции